纯净物
纯物质是均质的(即整个物质具有相同的化学成分),并且可以三相(气态、液态和固态)存在。纯物质的性质有助于理解热力学原理。
纯物质的共同性质包括:温度、压力、体积、质量、密度、比容、能量、焓和熵。这些属性可以分为广泛的或密集的。密集属性是一种不依赖于系统大小的属性。温度就是一个例子。广泛的属性是那些确实取决于系统大小的属性。示例包括质量和体积。
处理纯物质时的重要术语包括:
- 汽化,这是液体变成气相的点
- 冷凝,这是蒸汽变成液相的点(与汽化点相同)
- 熔化,这是固体变成液体的点
- 冻结,这是液体变成固体的点
- 升华,这是固体直接变成蒸气的点
- 凝华,这是蒸汽直接变成固体的点(不寻常但显然会发生)
- 临界点,是饱和蒸汽和饱和液体曲线相交并成为同一点。
- 三相点是固相、液相和气相同时存在且处于平衡状态的点。
Pv图细节
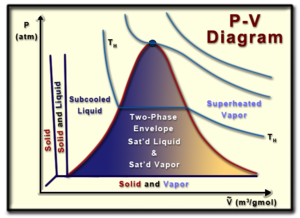
压力体积图(或 PV 图)是某种纯物质(均质物质)的压力和体积的直观表示。理解 PV 图有助于理解纯物质的性质,这是热力学的一个重要方面。
从图的顶部开始,临界点是物质的气相和液相之间没有区别的位置。此时饱和液体和饱和蒸气成为同一种流体,导致饱和液体和饱和蒸气的摩尔体积相等。
钟形曲线的左侧代表饱和液体线,而钟形曲线的右侧代表饱和蒸气线。饱和液体或蒸汽将位于其适当的线上,并且恰好是液体在现有压力下饱和或蒸发的位置。钟形曲线内部是所谓的两相包络线,其中物质的液相和气相同时存在。在这种状态下,物质具有某种质量 (x),其中物质的质量百分比是饱和蒸汽量与物质总质量的比率。数学质量可以定义为:
m
质量永远不能超过 100%。在两相包络中,重要的是要认识到温度和压力是相关的。在确定物质的状态时,不能同时指定压力和温度。
方程式
对于纯物质,有一些重要的方程式可以从 Pv 图或其在 Tv(温度-体积)、PT(压力-温度)图等中的变化来理解。
要确定混合物的总体积,首先要认识到这是液体所占体积的总和和气体所占体积的总和。这可以定义为:
mv = m f v f + m g v g
比容可以定义为:
v = v f +x*(v g -v f )
最后,认识到液体的质量百分比可以理解为 100(1-x),而蒸汽的百分比可以理解为 100x。
电视图
Tv 图展示了纯物质在温度和体积之间的关系。该图上的曲线是等压线或恒定压力线。在两相包络线下,尽管物质具有某种性质,但可以直接从图中读取饱和蒸汽或液体在一定压力下的摩尔体积。也就是说,饱和液体和饱和蒸气的性质与质量无关。
在此图中,两相包络线左侧的物质是过冷液体(因为温度低于饱和温度)。在两相包络的右侧,物质将是过热蒸汽(因为温度会高于饱和温度)。
PT图
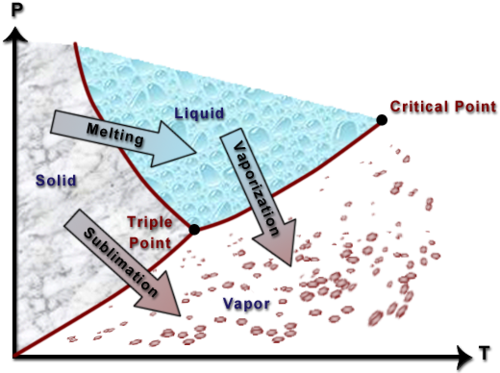
PT 图显示了压力和温度之间纯物质的关系。此图显示了冻结时膨胀的物质(例如水)的特性。
从该图中可以看出,液体的压力高于蒸气(蒸气压)。因此,液体可称为压缩液体。按照图表上的箭头演示需要做什么才能发生相变。例如,假设您在固体范围的中间存在水。如果你保持压力恒定并仅仅提高温度,固体就会熔化成液体。同样,对于大部分液体区域,如果在温度保持恒定的情况下降低压力,则液体会蒸发成气体。
参考
此页面上的所有信息均来自 www.learnthermo.com 和“工程师热力学,第二版”